info@genecompany.com|
基因快讯|


技术交流

扫描二维码
或添加“GeneGroup003”
获取更多更新资讯
商城订购

扫描二维码
或添加“基因商城(GeneMart)”
手机下单,快人一步
售后服务

扫描二维码
或添加“GeneGroup005”
获取更快速售后支持
LI-COR与Abcam公司强强联合,在JBC杂志联合发表关于抗体验证的文章

Western Blot是生命科学领域非常重要的一门技术,但是其结果由于多种因素的影响容易出现重复性差的问题。如何提高Western Blot实验的重复性是每一个科研人员包括期刊杂志都非常关注的问题,针对这个问题,2020年2月13日由LI-COR公司和Abcam公司在JBC杂志上联合发表题为【Antibody validation for Western blot: By the user, for the user】的文章,LI-COR作为全球近红外荧光成像领域的领导者,Abcam作为全球知名抗体公司,二者强强联合从抗体验证的角度阐述如何提高Western Blot重复性。
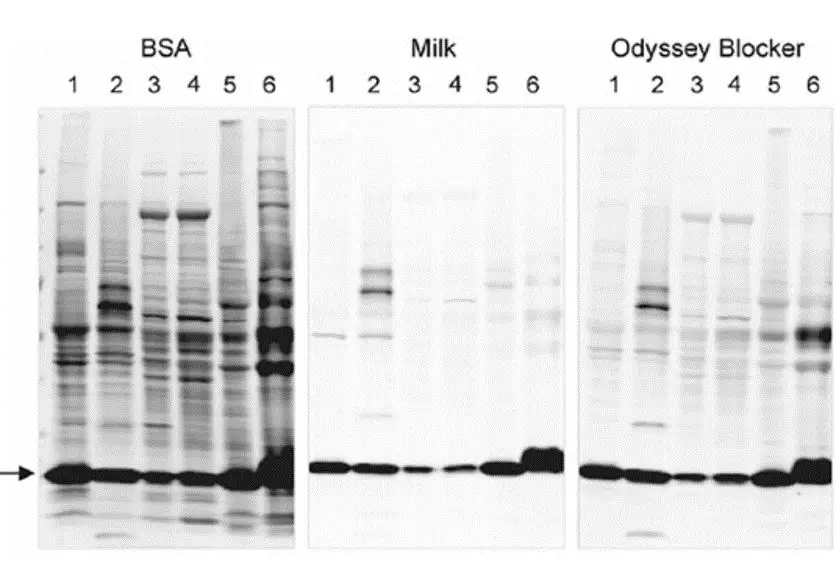
对于用户而言:不管抗体供应商有没有提供以上信息,用户也要对抗体进行验证,原因在于不能保证购买的抗体在用户端的实验中、对用户感兴趣的目标蛋白具有特异性。实验中的其他条件例如使用不同类型的封闭液也会对抗体的表现会产生影响。 Figure 2:不同类型封闭液对cofilin一抗性能的影响
使用合适的阳性对照和阴性对照对抗体的特异性和专一性进行验证。 阳性对照:阳性对照的结果正常,就表明整个实验体系、流程正常有效;反之整个实验体系、流程异常。 阴性对照:文中提到knock out (KO)和knockdown (KD)的细胞系/裂解液/组织是很好的阴性对照。RNAi-KD样品作为KO的替代品也可作为阴性对照(关于KO ,KD, RNAi-KD局限性详见原文)。
选择经过预吸附处理的抗体,经预吸附处理的抗体特异性更强。 对抗体的稀释度、浓度进行验证优化
多重Western Blot检测以及抗体验证 未来Western Blot检测的趋势是尽可能高通量地检测目标蛋白,而多重Western Blot可满足这个要求。 多重荧光Western Blot检测:允许在同一张膜上同时检测两种以上目标蛋白,不需要Stripping和Reprobing同时也避免了Stripping和Reprobing造成的假阳性和假阴性。LI-COR Odyssey Clx双色红外激光成像系统就可实现多重荧光Western Blot成像,重复性更好,定量更准确。 多重Western Blot检测中的抗体验证 对一抗和二抗进行验证以确认交叉反应是否影响Western Blot结果。 (1)首先在相似的实验条件下进行一抗的验证:将两种一抗混合后孵育进行Western Blot; 将两种一抗分别孵育进行Western Blot以验证是否有潜在的交叉反应或者干扰。 (2)二抗:可以通过识别不同的抗体种属对二抗进行验证。 Figure 7:PARPA1经星形孢菌素(STR)处理发生降解的多重近红外荧光Western Blot分析结果 备注:PARPA1经(STR)处理后会降解成85KD和25KD的两条条带,该实验在同一张膜上进行多种不同蛋白抗体特异性的验证; 泳道2、泳道3样本未经STR处理;泳道4、泳道5样本经过STR处理; A: 近红外荧光800nm通道:泳道2(未经STR处理的HAP1 WT样本),一抗ab32138在130kDa位置检测出全长PARP1蛋白 ;泳道4(经STR处理的HAP1 WT样本),一抗ab32138在130kDa位置检测出信号稍弱的全长PARP1蛋白,以及在28kDa位置检测出PARP1降解后N端条带(PARP1 p25); B: 近红外荧光700nm通道,泳道4(经STR处理的HAP1 WT样本),一抗ab110315在85kDa位置检测出PARP1降解后C端条带(PARP1 p85),在未经药物处理Control以及HAP1 PARP1KO样本中未检测出条带; C:近红外荧光700nm通道和800nm通道merge图像,清晰地检测出全长PARP1以及经STR处理后降解成85kD 、25kD两条条带。 以上Western Blot结果均在LI-COR Odyssey CLx近红外荧光成像仪上进行成像 实验更多详细信息详见原文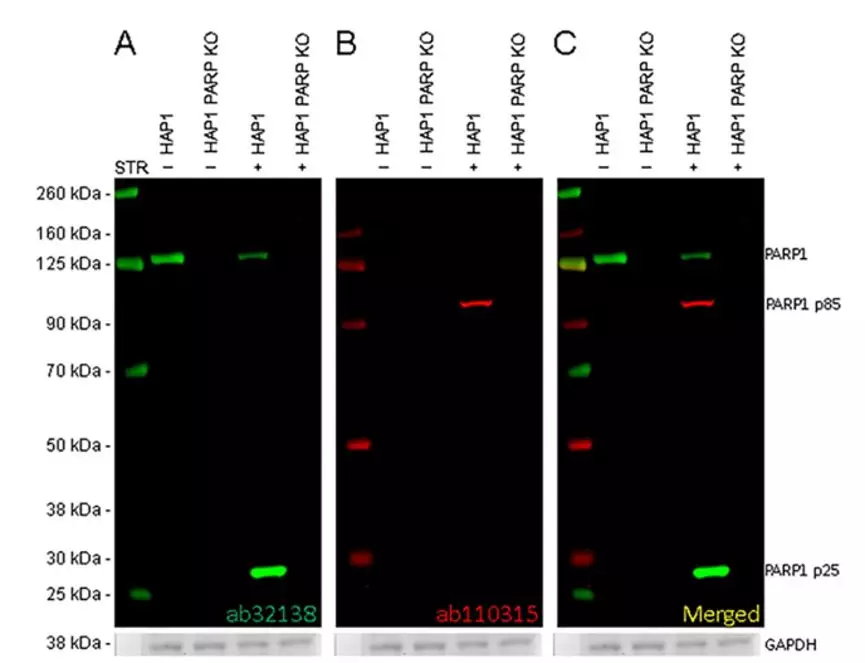
蛋白翻译后修饰研究(例如磷酸化修饰)中抗体验证的总原则: (1)目标蛋白总水平和目标蛋白翻译后修饰水平分别进行Western Blot以验证抗体的特异性; (2)对目标蛋白总水平和目标蛋白翻译后修饰水平的一抗分别用错配的/相反的二抗孵育进行Western Blot; (3)在特定实验条件下(例如药物处理)导致发生蛋白翻译后修饰,在上述条件下对目标蛋白翻译后修饰水平的一抗进行验证; (4)任何新的目标蛋白总水平和目标蛋白翻译后修饰水平的一抗,要设计多重Western Blot和两种蛋白单独实验进行抗体验证; ...... 更多详细内容请点击文末链接查看原文 备注: 在此文中共涉及Abcam 15种以上的一抗; 在此文所有的近红外荧光Western Blot结果均在LI-COR Odyssey CLx双色红外激光成像系统进行成像,并用LI-COR的ImageStudio 5.2版本的软件进行数据分析。
关于LI-COR Biosciences
LI-COR Biosciences公司作为近红外荧光成像的创始者和领导者,在近红外荧光成像领域已有25年的丰富历史,是名副其实的近红外专家。 25年来,LI-COR Odyssey ®双色红外激光成像系统由于可实现Western Blot精确定量,进行多重Western Blot,提高重复性,得到了全球生物医学研究人员的信赖。 极其丰富的应用

LI-COR Biosciences公司作为近红外荧光成像的创始者和领导者,在近红外荧光成像领域已有25年的丰富历史,是名副其实的近红外专家。LI-COR 与基因有限公司的终极目标是希望帮助您解决Western Blot实验中的问题,帮助您获得符合杂志发表的可重复数据。 基因有限公司作为LI-COR产品中国区独家代理商,与LI-COR一起邀请您一同关注近红外荧光成像技术在Western Blot准确定量、磷酸化等蛋白修饰化研究、In-Cell Western、双色EMSA、蛋白芯片及光免疫疗法等方面的应用进展。欲进一步了解详细内容,请关注我们的官方微信“基因快讯”或联系您身边的基因有限公司工作人员。
原文链接:https://www.jbc.org/content/295/4/926.full.pdf?sid=4eb69491-ff6e-4b88-96e3-c36d98f9c77f
参考文献:
[1]PillaiKastoori, L. and Heaton, S. et al., 2020.Antibody Validation for Western blot: By the User, for the User.J Biol Chem. 295(4): pp YY-Z.
[2]Lithgow, G. J., Driscoll, M., and Phillips, P. (2017) A long journey to reproducible results. Nature 548, 387–388 CrossRef Medline
[3]Uhlen, M., Bandrowski, A., Carr, S., Edwards, A., Ellenberg, J., Lundberg, E., Rimm, D. L., Rodriguez, H., Hiltke, T., Snyder, M., and Yamamoto, T. (2016) A proposal for validation of antibodies. Nat Methods 13, 823–827 CrossRef Medline