info@genecompany.com|
基因快讯|


技术交流

扫描二维码
或添加“GeneGroup003”
获取更多更新资讯
商城订购

扫描二维码
或添加“基因商城(GeneMart)”
手机下单,快人一步
售后服务

扫描二维码
或添加“GeneGroup005”
获取更快速售后支持
新冠肺炎核酸检测假阴性,症结在这里

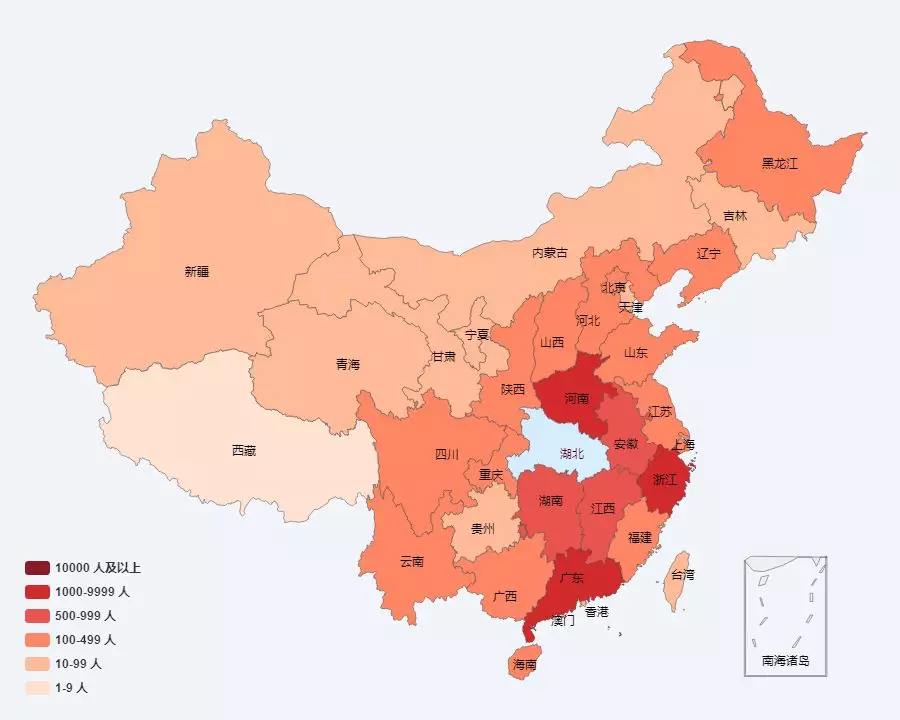
更近几天,备受民众和媒体关心的问题之一就是新冠肺炎的病毒核酸检测假阴性。 主要与流感病毒、副流感病毒、腺病毒、呼吸道合胞病毒、鼻病毒、人偏肺病毒、SARS冠状病毒等其他已知病毒性肺炎鉴别,与肺炎支原体、衣原体肺炎及细菌性肺炎等鉴别。此外,还要与非感染性疾病,如血管炎、皮肌炎和机化性肺炎等鉴别。
因此,核酸检测目前仍然是更准确的诊断方法。
关于这些问题,网络上充斥着各种声音。
我们把这个流程划分为三个环节:采样及运输环节、核酸提取环节和qPCR检测环节。
因此,样本采集是一个主要因素。
2、核酸提取环节
注意,这个环节从样本灭活开始,到获得样本中RNA结束。而且样本具有特殊性。
3、qPCR检测环节
首先我们需要明确的是,要有病毒核酸存在,qPCR才能检测出来。有专家在质疑检测试剂盒的质量以及检测手段,认为应该对不同厂商的试剂盒进行系统对比,我们赞成这个做法,因为不排除有试剂盒原料、引物设计、产品质控手段及产品批次间有差异。但是我们也要为大部分试剂盒生产厂家和仪器生厂商说句公道话:qPCR方法诞生于1996年,发展至今技术非常成熟,检测灵敏度可低至1个拷贝,是当今应用于临床的更先进的核酸分子诊断技术之一。
因此,在qPCR 检测环节,检测试剂盒是一个因素,还有一个影响因素是检测技术人员的技术水平。值得庆幸的是,这两个影响因素随着试剂盒质量和技术人员水平的不断提升正在逐渐减少。
经过总结,我们不难发现,在整个新冠肺炎样本进行核酸检测过程中,导致假阴性结果的主要因素有4个:1、样本采集;2、病毒核酸提取前的样本处理方法;3、检测试剂盒质量;4、操作人员水平。
经过前面讨论,现在更关键的影响因素已经浮出水面了,那就是样本采集和病毒核酸提取之前的样本处理方法。也就是说如果没有采集到样本或者没有提取到病毒的核酸分子,再牛的检测试剂盒结果也只能是阴性。
临床样本采集有先天的局限性,可以说有很大一部分的假阴性是因为只采集到一点点的带病毒样本,这一点点样本还有很多黏蛋白,很难裂解,想要提取到核酸还得能用于qPCR扩增可以说是非常困难的,假阴性的结果也变成情理之中了。
每一份痕量珍贵的样本背后,都有一个亟待救治的患者,每一份检测报告的背后,都是不止一位检测工作者超过5个小时的风险操作。
痕量黏性样本,如何阴转阳?我们大胆的提议:
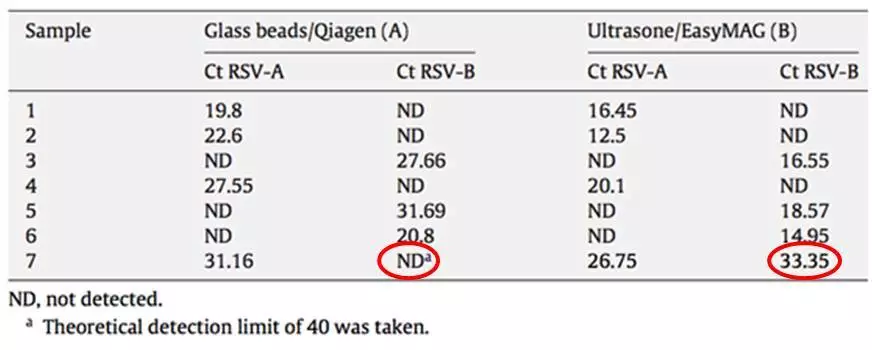
下面这个分枝杆菌鉴定的案例,也充分证明了这一点。
分枝杆菌
常规方法(高温灭活和珠子处理)完成一次菌株灭活及多肽提取需要95.5分钟,其中95℃灭活30分钟,使用聚焦超声技术完成一次菌株灭活及多肽提取仅需4.5分钟,其中18℃灭活仅需2分钟,接受测试的21个种属182份样品在2分钟处理条件下完全灭活。比传统方法节约28分钟。
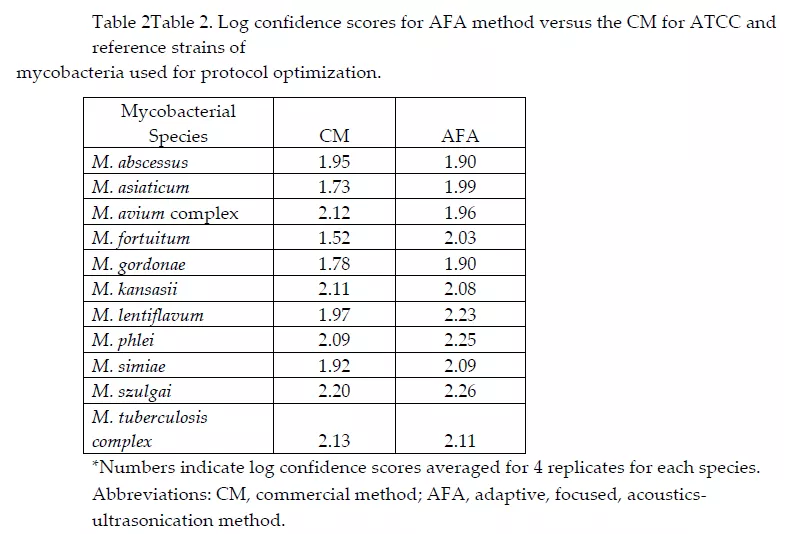
(注:得分表示未知样品的质谱图谱与数据库中已知样品的图谱的相似程度,Log值越高,表明待测样品的细菌蛋白质鉴定的灵敏性和准确度越高)

基于聚焦超声技术的高性能样本处理方法
Adaptive Focused Acoustics™,AFA
滑动查看Covaris 各型号仪器
如果您的实验室里有以上仪器,并且您的实验室正在进行新冠肺炎病毒相关的检测工作,我们愿意为您提供我们能力范围内更大的支持,与您一起,攻克难关。
参考文献:
David Nauwelaersa,∗, Leen Vijgenb et al. "Development of a real-time multiplex RSV detection assay for difficult respiratory samples, using ultrasone waves and MNAzyme technology" Journal of Clinical Virology 46 (2009) 238–243
La’Tonzia, L. Adams, et al. "A Rapid Standardized Protein Extraction Method Using Adaptive Focused Acoustics for Identification of Mycobacteria by MALDI-ToF MS." Diagnostic Microbiology and Infectious Disease (2016).