info@genecompany.com|
基因快讯|


技术交流

扫描二维码
或添加“GeneGroup003”
获取更多更新资讯
商城订购

扫描二维码
或添加“基因商城(GeneMart)”
手机下单,快人一步
售后服务

扫描二维码
或添加“GeneGroup005”
获取更快速售后支持
Cytation系统在3D细胞研究中的应用分享(二)

3D细胞作为细胞学研究中必不可少的研究工具,具有比2D细胞更加仿生的自然环境,能够更加准确地模拟体内细胞的行为,建立细胞-细胞和细胞-细胞外基质(ECM)之间的通讯网络,弥补了单层细胞培养的缺陷。在之前的分享中,关于Cytation系统在3D细胞研究中的应用分享已经做了初步的介绍,今天,我们将进一步分享3D细胞研究的相关应用。 应用分享 应用一 利用自动成像和先进的3D细胞培养技术量化凋亡活性
凋亡,或细胞程序性死亡,对所有多细胞生物的正常发育和内稳态至关重要,是对抗癌症的一个关键研究工具。然而,在细胞凋亡研究中培养细胞模型仍存在挑战,传统的2D细胞培养方式缺乏仿生环境,会导致分化细胞功能和代谢能力的丧失,新颖的3D细胞培养方式具有细胞-细胞和细胞-细胞外基质(ECM)之间的相互作用,并使得细胞形态和行为更接近体内真实状态,更有利于研究肿瘤细胞的作用机制和耐药性。因此,本研究展示了一种新型的3D细胞培养模型Elplasia®,用于阐明两种化合物在两种不同细胞系中的凋亡潜能,并通过Cytation系统进行自动成像和凋亡活性的量化分析。
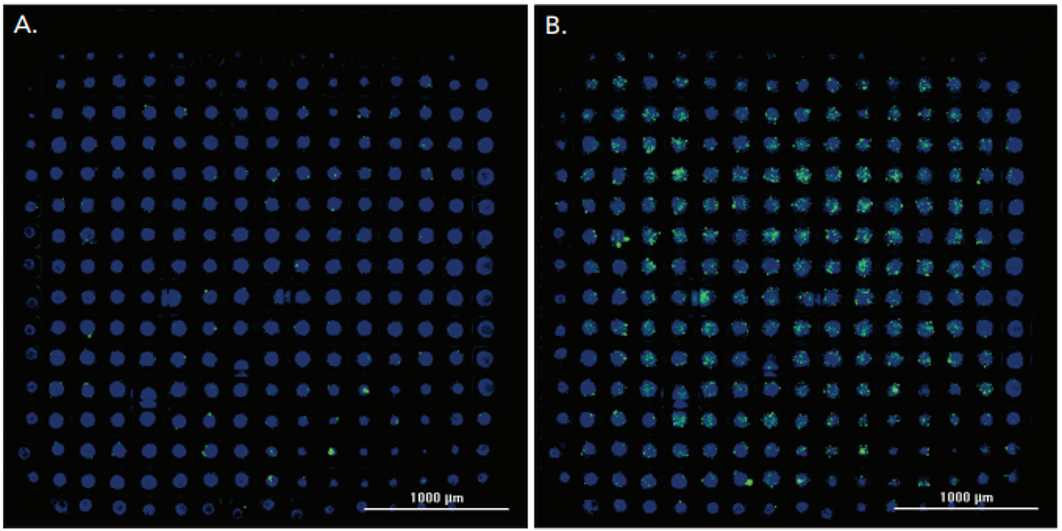
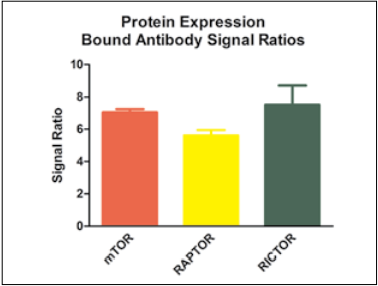
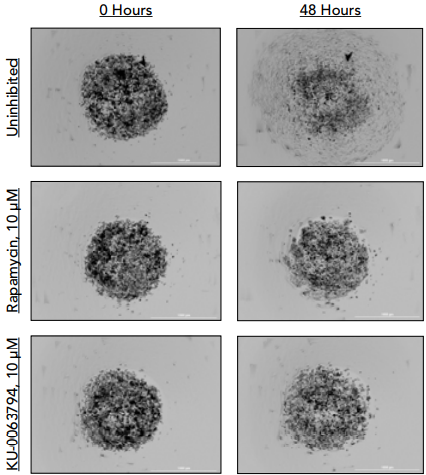
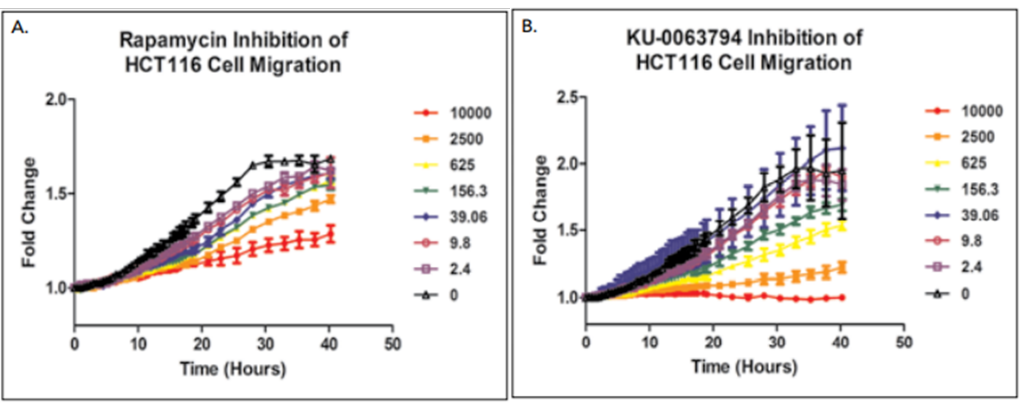
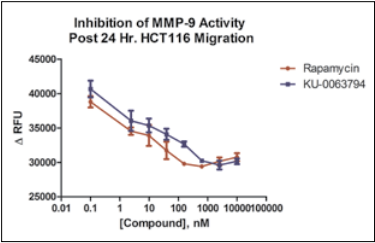
1 材料方法 基于Elplasia® 384孔黑壁透明底的超低吸附微孔板,采用Abcam®凋亡动力学试剂盒检测盐酸阿霉素和冬凌草甲素对HT-1080纤维肉瘤细胞和HCT116结直肠癌细胞的凋亡活性影响。 2 结果分析 磷脂酰丝氨酸(PS)外翻是细胞早期凋亡的标志,pSIVE-IANDB荧光探针与PS结合产生强烈的绿色荧光信号,可用于监测细胞凋亡,从而使用该探针检测HCT116和HT-1080 3D细胞球的凋亡活性。如图1 所示,400 nM阿霉素处理HT-1080 3D细胞球,在24小时几乎看不到信号,但在48小时显示出高水平的绿色荧光,表明其凋亡水平的增加。 图1. 400 nM阿霉素处理HT-1080 3D细胞球的凋亡活性。 利用集成的Gen5数据分析软件对每孔随时间变化的凋亡球体数目进行测定,并通过归一化分析,计算每个孔中凋亡球体的百分比,如图2所示。 图2.动态显示10 µM浓度的阿霉素或冬凌草甲素处理的HCT116或HT-1080 3D细胞球的凋亡百分比。 最后,通过终点法分析,以比较这两种细胞系在特定化合物浓度和孵育时间下的凋亡活性,如图3所示,化合物对HT-1080细胞表现出更强的凋亡效应,而当化合物浓度高于1000 nM时,细胞凋亡活性下降,很可能是每个球体内的细胞坏死所致。相比之下,HCT116细胞对这两种化合物的抗性更强,因此需要更高的化合物浓度来诱导凋亡反应。 图3.不同浓度阿霉素或冬凌草甲素处理48小时后 HCT116或HT-1080 3D细胞球的凋亡百分比。 该研究通过Cytation系统和Elplasia®超低吸附球形微孔板,可以从单个细胞类型和药物组合中检测到特异性的表型凋亡效应,提供了一种简单、快速、灵活、准确的方法来评估抗癌药物基于靶向和表型效应的分析。 应用二 利用3D生物打印结直肠癌细胞自动监测蛋白质表达和转移性细胞迁移 结直肠癌(CRC)是最常见的癌症类型之一,对于晚期结直肠癌患者,由于肿瘤易转移和对治疗的抵抗,导致生存率很低。先前的研究表明雷帕霉素丝氨酸/苏氨酸激酶哺乳动物靶点(mTOR)的两个复合物mTORC1(含RAPTOR)和mTORC2(含RICTOR)在CRC中过表达,并在肿瘤的发生和转移中起作用,此外,mTOR信号通路的上调也可以诱导基质金属蛋白酶(MMPs)的表达,而MMPs也在CRC转移中发挥作用。因此,开发含有mTOR抑制剂的治疗方法可能会降低这种癌症的转移潜力并提高生存率。由于结直肠癌在体内是以三维(3D)实体瘤的结构生长,而对CRC研究的一个主要限制因素是使用二维(2D)培养的细胞,因此,本研究通过一种磁性3D生物打印细胞培养平台进行结直肠癌细胞蛋白质表达评价和转移性细胞迁移研究。 1 材料方法 将HCT116上皮结直肠癌细胞、CCD841 CoN结肠上皮细胞分别与表达RFP的人新生儿皮肤成纤维细胞共培养,通过免疫荧光染色检测mTOR及其复合物蛋白的表达;加入mTOR抑制剂雷帕霉素和KU-0063794,检测细胞迁移情况及MMPs活性。 图1. 磁性3D细胞生物打印方法。 2 结果分析一 蛋白表达分析 对HCT116/成纤维细胞和正常结肠/成纤维细胞共培养球体模型进行免疫荧光染色发现,在正常和病变球体模型中,结肠上皮细胞和成纤维细胞之间的细胞组织存在差异。HCT116细胞和成纤维细胞以相互排斥的方式组织,其中癌细胞层位于成纤维细胞核的顶部(图2A),而正常结肠细胞和成纤维细胞以一种包容的方式组织,促进每种细胞类型在球体内的均匀分布(图2B)。 图2.免疫荧光检测和分析。 然后测定每个球体内的蛋白表达,根据共培养细胞球体的综合Cy5荧光信号进行分析,如图3。结果显示,与正常结肠细胞相比,病变结肠上皮细胞球体模型中的mTOR、RAPTOR和RICTOR蛋白表达增加了8倍之多,与之前研究结果一致。该结果也进一步证实了3D共培养的HCT116/成纤维细胞球体模型非常适合用于体外研究。 图3.蛋白表达量化分析。 3 结果分析二 细胞迁移与MMPs活性分析 为探究mTOR抑制剂对癌症转移的影响,进一步通过mTOR抑制剂雷帕霉素和KU-0063794处理3D打印的结直肠癌细胞,结果发现,在未处理的3D细胞中,细胞和基质随着时间的推移远离原始打印区域,而10 μM浓度的雷帕霉素或KU-0063794则完全抑制迁移(如图4)。 图4. HCT116细胞迁移分析。 通过Gen5软件对不同浓度的雷帕霉素和KU-0063794进行细胞迁移分析发现,雷帕霉素和KU-0063794对HCT116细胞的迁移能力均有剂量依赖性影响,与雷帕霉素相比,KU-0063794在10 μM浓度时具有更完整的抑制作用(图5),这可能是由于雷帕霉素仅急性抑制mTORC1,而对mTORC2作用甚微,而KU-0063794是已知的两种mTOR复合物的抑制剂。当然,为排除细胞增殖产生的影响,在孵育前后通过测量细胞的ATP水平对细胞活性进行了评估。 图5. HCT116细胞迁移的动力学分析。 由于MMPs的产生受mTOR信号通路的调控,并在CRCs的侵袭和迁移中发挥作用,因此,该研究也对MMPs的活性进行检测(图6),可以确定,雷帕霉素或KU-0063794对MMP-9的活性也起了抑制作用。 图6. MMP-9活性分析。 该研究提供了一种简单、可靠的方法创建3D细胞球体模型,可准确评估正常和病变3D细胞模型之间的蛋白表达变化,以及抑制细胞信号通路对转移细胞迁移的影响。 基因有限公司作为Agilent BioTek在中国的合作伙伴,致力于为您提供更加完备的自动化成像检测系统。邀您一同关注我们的官方微信“基因快讯”,如需要了解更多产品信息,可留言或者直接联系基因有限公司。