info@genecompany.com|
基因快讯|


技术交流

扫描二维码
或添加“GeneGroup003”
获取更多更新资讯
商城订购

扫描二维码
或添加“基因商城(GeneMart)”
手机下单,快人一步
售后服务

扫描二维码
或添加“GeneGroup005”
获取更快速售后支持
实体瘤单细胞DNA建库怎么做?自动化组织解离+微流控技术来帮你!


实体瘤单细胞DNA建库方案 从单细胞基因组技术面世的十年以来,研究者们一直致力于提高单细胞研究的通量和分辨率。相较于传统的bulk测序而言,单细胞DNA分析改变了癌症研究的发展方向,避免了正常细胞和肿瘤细胞的信号混合,可以区分肿瘤内部不同的的亚克隆,这样可以对单个肿瘤内的不同克隆谱系进行识别,加强了肿瘤异质性的高分辨率洞察,帮助理解癌症的进化和靶向治疗决策。基于现有实体瘤单细胞测序预处理工作流程往往不能提供足够的细胞或细胞核数据,进而无法提供有意义的结果。 Mission Bio于2022年4月正式携手实验室自动化解决方案开发商S2 Genomics,致力于简化从实体瘤样本制备到单细胞DNA分析的工作流程,提供自动化的实体瘤样品预处理解决方案。研究人员现在可以将S2 Genomics的Singulator 100组织解离技术与Tapestri微流控自动化建库方案搭配使用,在同一工作流程中进行可扩展的、高产的、高效且可重复的单细胞DNA建库。 同时Mission Bio三月正式推出了首个用于实体瘤研究的Tapestri解决方案,其中包括针对乳腺癌和多形性胶质母细胞瘤的新型预设计Panel,以及升级版的单细胞拷贝数变异(CNV)生信分析工具。 应用分享

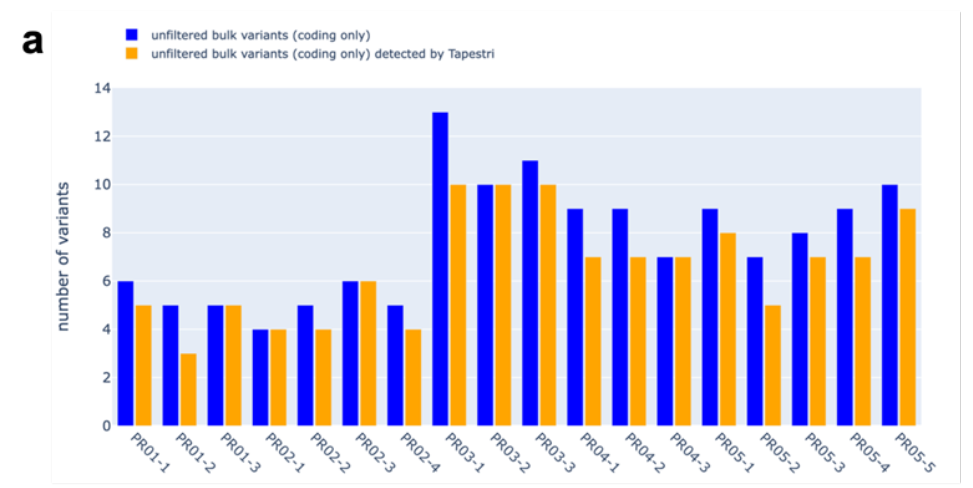
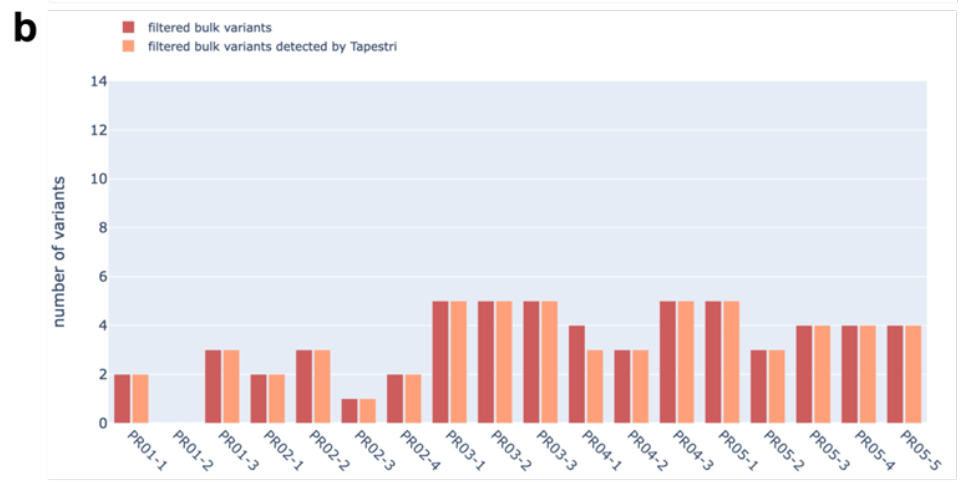
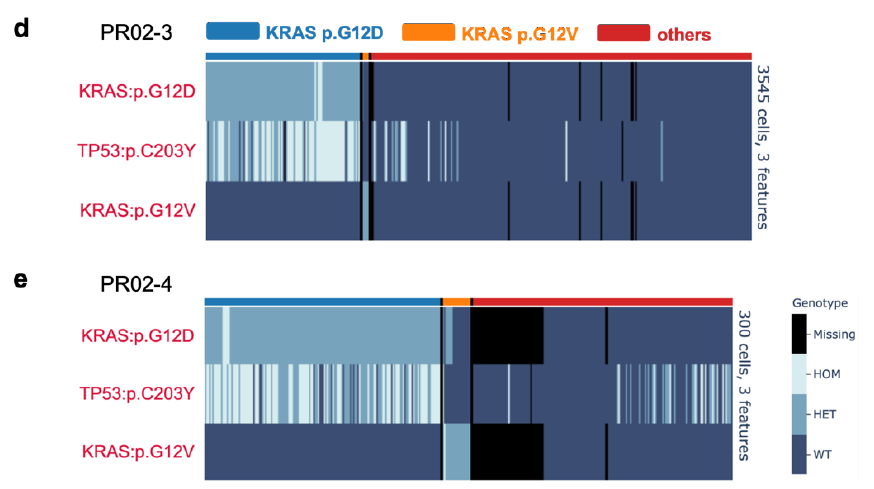
上述自动提取细胞核和分析工作流程已由纪念斯隆凯特琳癌症中心(Memorial Sloan Kettering Cancer Center,简称MSKCC) 胰腺癌研究中心主任Christine A. Iacobuzio-Donahue博士实验室进行分析验证,最新发现已在美国癌症研究协会 (American Association for Cancer Research,简称AACR) 年会上发表。该研究获取了16例胰腺导管腺癌(PDAC)病人的原发灶和转移灶共34个部位。使用S2进行冻存组织的自动化解离和细胞核提取,后续在Mission Bio Tapestri平台构建了38个单细胞核DNA(snDNA)文库,并在NGS平台测序,每个文库平均获得了2867个细胞核的数据。 组织单细胞DNA测序流程 工作流程评估 该研究使用186个扩增子panel覆盖93个常见突变位点,对该工作流程的可行性和数据的可靠性进行了评估: 为了验证Tapestri微流控工作流程的可行性,作者选取了两个含有不同驱动突变(TP53 . c207y vs. ARID1A splice)的患者,通过bulk WES和Tapestri snDNA-seq 进行了正交验证来评估双包率。根据两个驱动突变的基因型将每个细胞分配给两个原始肿瘤。利用混合模型,根据携带两种肿瘤体细胞变异的条形码数量,推导出双包率为3-5%。 双包率验证结果 2、单核苷酸变异评估 为了评估snDNA-seq在检测SNV的稳健性,作者选取了18个样本的数据与之前的bulk WES数据进行比较,发现单细胞测序panel包含的基因突变与WES中对应基因突变具有良好的一致性。 snDNA-seq与Bulk WES检测到的变异数目对比(a:数据未过滤;b:数据过滤后) 3、拷贝数变异评估 接下来作者试图确定snDNA-seq方法是否可以检测在低深度/低覆盖率的bulk seq数据中可能难以调用的亚克隆拷贝数变异(CNVs),所以对已知SMAD4和CDKN2A纯合缺失PA02-1号样本进snDNA-seq数据分析,计算单细胞中相应扩增子reads数目和倍性关系,发现这两个基因部分外显子的纯合缺失存在于有KRAS突变的肿瘤克隆(占28.5%)中。 PA02-1号病人的SMAD4和CDKN2A突变情况 4、snDNA-seq在低细胞量、低肿瘤含量样本的可行性评估 作者使用PA04-1号的低肿瘤细胞含量的原发胰腺癌肿瘤样本(组织脂肪含量高,肿瘤细胞在切片上显示小于50%面积),使用约8平方毫米的组织使用Sigulator 100提取到了30000个细胞核上机建库,高质量地读取了肿瘤克隆中的两个驱动突变(KRAS p.G12V,SMAD4 p.A39T)。 PA04-1号样本低起始量scDNA-seq 重要结论 1、snDNA-seq鉴定两种KRAS互斥突变 对于一例手术切除多病灶病例PR02,WES发现其存在KRAS p.G12D热点突变,和KRAS p.G12V突变(该突变处于技术检测灵敏度的边缘)。单细胞数据发现KRAS p.G12D和TP53 p.C203Y共突变的存在,并且发现KRAS p.G12V与上述两种突变的互斥现象。在PR02-4中,KRAS p.G12V 次要克隆只有12个细胞(0.33%),证明了scDNA-seq技术的灵敏性。 2、snDNA-seq发现KRAS-WT 病人中复杂的克隆结构 研究表明大于90%的PDA都存在KRAS突变,但是该研究中PR01病例的WES数据显示,该病例三个不同病灶的样本都呈现KRAS WT。对三个不同空间位置的PR01样本进行snDNA-seq,发现了FGFR1突变和TGFBR2突变分别存在于两个互斥的克隆,这两个克隆有许多共有的CNVs,说明这两个克隆源于一个祖克隆,并且CNV的发生先于SNV。 PR01-3 7个热点突变基因scDNA-seq基因型热图 TGFBR2和FGFR1克隆的CNVs 3、snDNA-seq揭示肿瘤的逐步进化 通过对PA04样本的一个原位和两个肝转移样本进行snDNA-seq,根据KRAS和SMAD4两个基因型鉴定了5个不同的亚克隆,并根据突变的互斥和共现、突变的合子性和突变细胞的比例等信息推断出肿瘤的逐步进化过程和转移发生的时间点。 PA04号病人的肿瘤克隆进化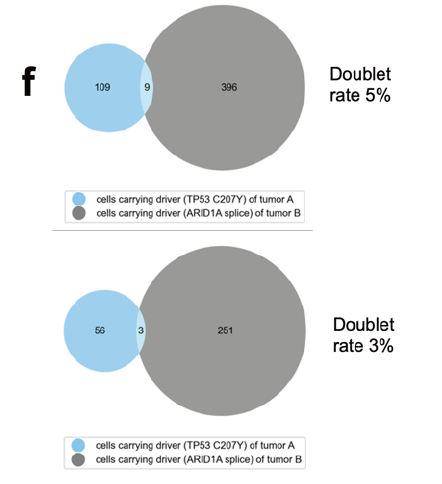
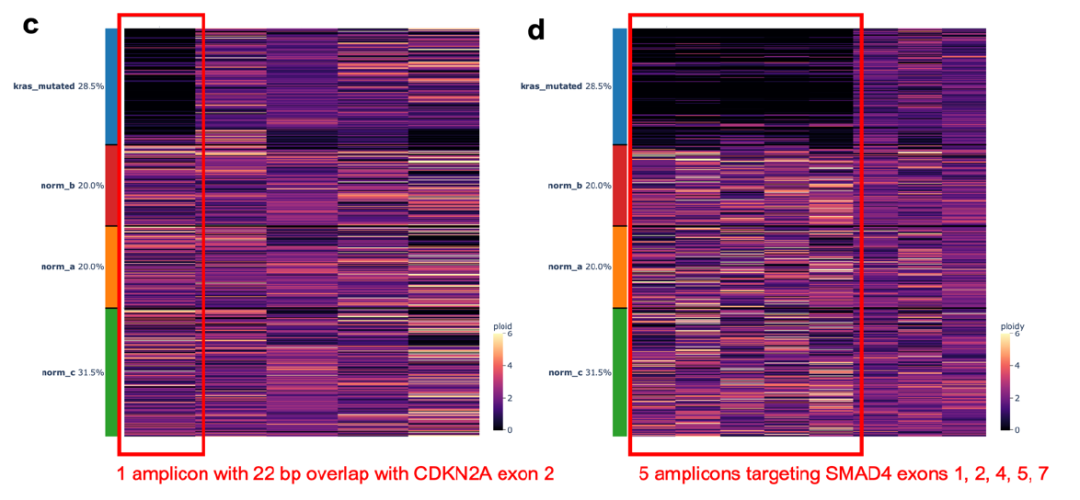
在某些临床情况下,如细针穿刺、针芯活检获得的细胞有限,给bulk测序带来非常大的障碍,作者想验证这种低起始细胞量的情况是否在Tapestri上可行。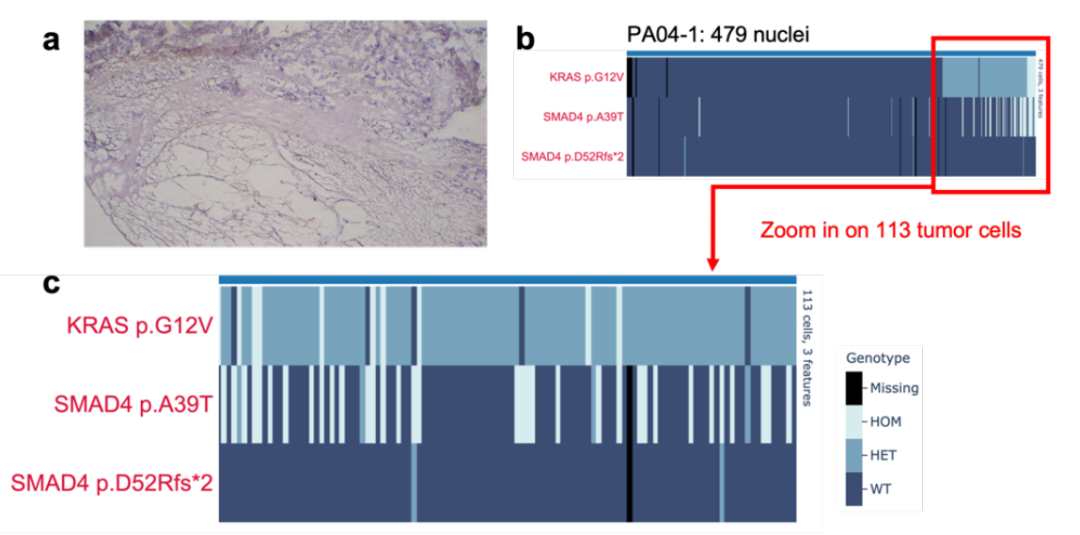
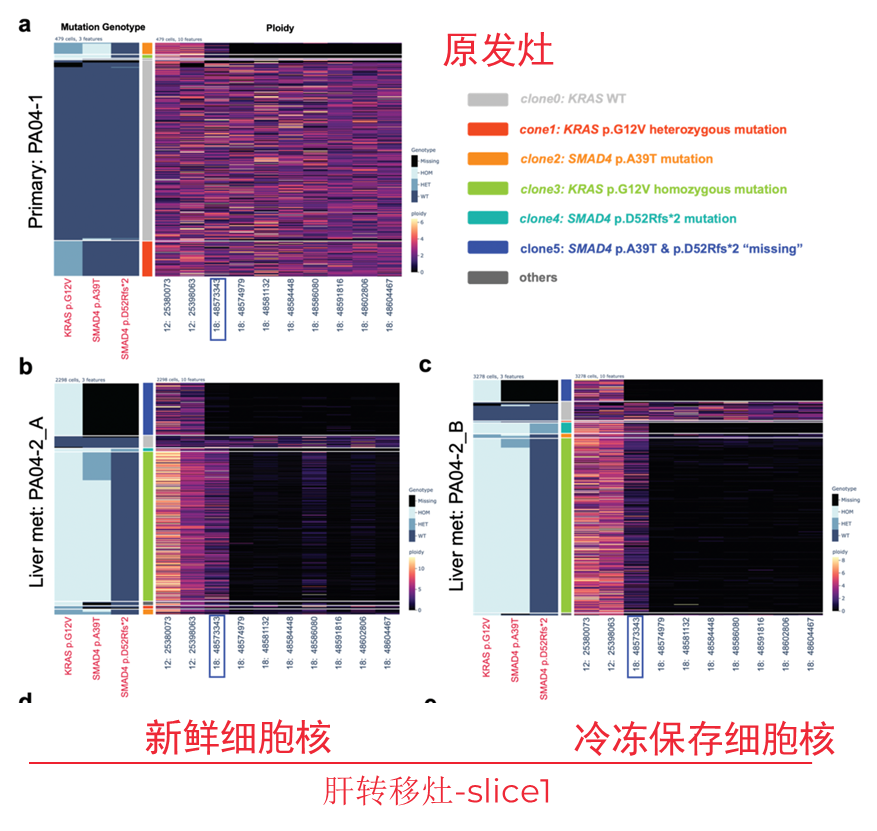
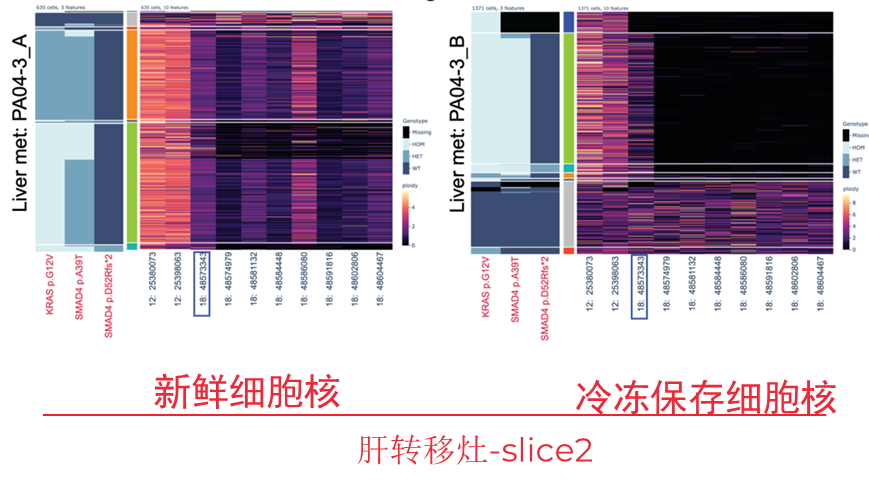
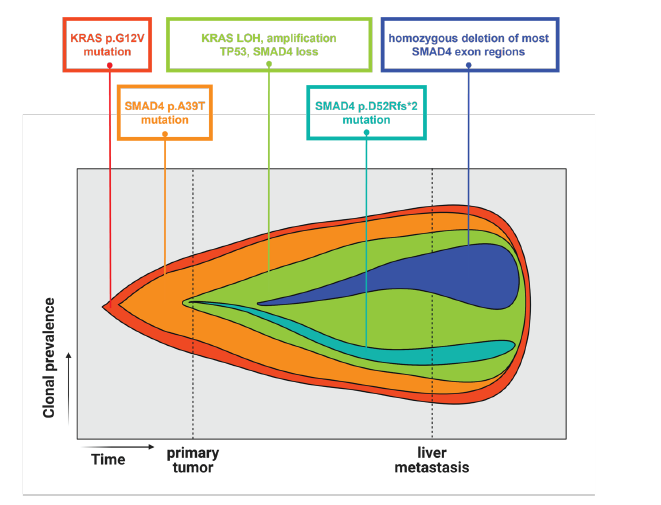
总之,在这项研究中,作者使用两种商品化的平台进行了高度自动化的工作流程,从快速冷冻的患者组织中或者冻存的单细胞核悬液中生成Tapestri snDNA-seq文库。该工作流程快速、高效,可用于高通量的临床和转化研究。
联系我们 基因有限公司于2022年正式成为美国Mission Bio公司的合作伙伴,并且代理S2 Genomics Sigulator 100产品,提供两个平台的售前技术咨询、售后安装培训、应用支持等工作。期待和更多领域先锋一道,攻克疾病研究难题,造福更多患者。如果您对单细胞多组学感兴趣,可以扫描左边二维码进行一对一沟通,或联系您身边的“基因人”。